SSM@100Hz con FibroScan® Mejora el Diagnóstico No Invasivo de la Hipertensión Portal Clínicamente Significativa, Respaldando su Implementación en la Práctica Clínica

Referencia del estudio
Jachs, et al. Spleen stiffness measurement by vibration-controlled transient elastography at 100 Hz for non-invasive predicted diagnosis of clinically significant portal hypertension in patients with compensated advanced chronic liver disease: a modelling study. The Lancet 2024
| Tipo de población | Enfermedad hepática crónica avanzada compensada (cACLD) debido a: MASLD (40%): Enfermedad hepática esteatósica asociada a disfunción metabólica. MetALD o ALD (33%): Enfermedad hepática relacionada con disfunción metabólica e ingesta de alcohol o únicamente por alcohol. Hepatitis viral (18%). Otras enfermedades hepáticas crónicas (9%) |
| Tamaño de la muestra | 407 pacientes con cACLD provenientes de 16 centros especializados en Europa entre el 1 de enero de 2020 y el 31 de diciembre de 2023 |
| Objetivo principal | Evaluar la utilidad diagnóstica de la medición de la rigidez del bazo (SSM) a 100 Hz como prueba no invasiva independiente para la hipertensión portal clínica significativa (CSPH). Además, analizar su valor incremental en comparación con el modelo ANTICIPATE±NASH en pacientes con cACLD |
| Resultado principal | Hipertensión portal clínica significativa (CSPH) |
| Acrónimos | AUC: Área Bajo la Curva MASLD: Enfermedad hepática esteatósica asociada a disfunción metabólica MASH: Esteatohepatitis asociada a disfunción metabólica MetALD: Enfermedad hepática esteatósica asociada a disfunción metabólica con aumento en la ingesta de alcohol ALD: Enfermedad hepática alcohólica cACLD: Enfermedad hepática crónica avanzada compensada CSPH: Hipertensión portal clínicamente significativa SSM: Medición de la rigidez del bazo LSM: Medición de la rigidez hepática VCTE: Elastografía de transición por vibración controlada HVPG: Gradiente de presión venosa hepática Modelo NICER: Modelo de riesgo estimado no invasivo para CSPH |
Antecedentes y objetivo
La hipertensión portal clínica significativa (CSPH, por sus siglas en inglés) es una complicación grave de la enfermedad hepática crónica avanzada compensada (cACLD) que aumenta significativamente el riesgo de morbilidad y mortalidad.
El estándar de oro actual para diagnosticar CSPH es la medición invasiva del gradiente de presión venosa hepática (HVPG), la cual no es ampliamente accesible fuera de los centros especializados.
Para abordar esta limitación, el comité Baveno VII recomendó el uso de pruebas no invasivas para estimar la probabilidad de CSPH y guiar la necesidad de tratamiento con bloqueadores β no selectivos, como el carvedilol.
Estas pruebas, incluidas las basadas en los modelos ANTICIPATE y ANTICIPATE-NASH, se fundamentan en la medición de la rigidez hepática (LSM), el recuento de plaquetas y, en pacientes obesos con MASH, el índice de masa corporal (IMC). Sin embargo, estas pruebas enfrentan limitaciones debido a la incertidumbre diagnóstica en ciertos grupos de pacientes.
Recientemente, la medición de la rigidez del bazo (SSM) mediante elastografía de transición por vibración controlada (VCTE™) a 100 Hz ha mostrado ser una alternativa confiable y no invasiva, especialmente cuando se combina con otros marcadores.
Este estudio evaluó el SSM por VCTE™ a 100 Hz como una prueba independiente, combinada con el recuento de plaquetas e IMC, y como parte del modelo integral de riesgo estimado no invasivo para CSPH (NICER), que integra SSM, LSM, recuento de plaquetas e IMC (ver Fig. 1).
Figure 1. Nomogram of NICER model predicting CSPH in patients with compensated advanced chronic
Metodología
Un total de 407 pacientes con diversas enfermedades hepáticas crónicas y cACLD fueron reclutados de 16 centros especializados en toda Europa entre el 1 de enero de 2020 y el 31 de diciembre de 2023.
Los pacientes se dividieron en dos grupos: una cohorte de derivación (2020–2022) y una cohorte de validación (2023). Cada paciente se sometió a una medición de HVPG, SSM mediante VCTE a 100 Hz, LSM mediante VCTE™ a 50 Hz y pruebas de recuento de plaquetas.
La medición de HVPG se utilizó como estándar de referencia para diagnosticar hipertensión portal clínica significativa (CSPH), definida como HVPG ≥10 mmHg.
Resultados principales
Se evaluaron tres modelos en el estudio: SSM como prueba independiente, LSM combinado con el recuento de plaquetas e IMC (modelo ANTICIPATE-NASH), y un modelo integral que integra SSM, LSM, recuento de plaquetas e IMC (modelo NICER).
El SSM mediante VCTE a 100 Hz demostró ser una herramienta no invasiva altamente precisa para diagnosticar CSPH en pacientes con cACLD.
Entre los modelos, el modelo NICER superó al modelo ANTICIPATE-NASH existente, logrando una precisión diagnóstica superior con un área bajo la curva (AUC) de aproximadamente 0.9 en ambas cohortes, tanto la de derivación como la de validación (ver Tabla 1).
| Predicción de CSPH (AUROC) | Cohorte de derivación | Cohorte de validación |
| SSM | 0.779 | 0.830 |
| LSM | 0.718 | 0.804 |
| SSM, PLT, BMIH | 0.849 | 0.873 |
| ANTICIPATE +/- NASH | 0.849 | 0.863 |
| Modelo NICER | 0.889 | 0.906 |
Tabla 1. Medidas de rendimiento diagnóstico de los criterios de Baveno VII y algoritmos de diagnóstico que consideran el SSM en las cohortes de derivación y validación
En la cohorte de validación, los criterios de Baveno VII lograron descartar con precisión la CSPH, con una alta sensibilidad (99.2%) para excluirla y una alta especificidad (91.1%) para confirmarla. Sin embargo, un número significativo de pacientes permaneció en la zona gris diagnóstica (54%).
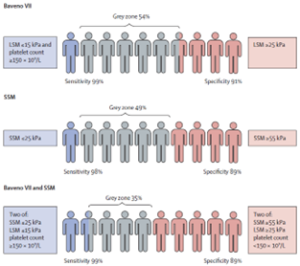
Los puntos de corte de SSM propuestos por Baveno VII (21 kPa y 50 kPa) mostraron una sensibilidad aceptable, pero una especificidad baja, que podría mejorarse ajustando los puntos de corte a 25 kPa y 55 kPa, manteniendo zonas grises similares (ver Fig. 2).
Figura 2. Rendimiento de los puntos de corte para confirmar y descartar hipertensión portal clínica significativa: Baveno VII y SSM en la cohorte de validación
Mensajes clave
- Los pacientes incluidos en el estudio presentaron MASLD (40%), MetALD o ALD (33%), hepatitis viral (18%) y otras enfermedades hepáticas crónicas (9%), lo que demuestra la aplicabilidad de estas herramientas diagnósticas en diversas condiciones hepáticas.
- La adición de SSM al LSM, IMC y recuento de plaquetas (modelo NICER) superó al modelo ANTICIPATE±NASH para la estratificación del riesgo de CSPH en pacientes con cACLD, mostrando que el SSM mejora el diagnóstico no invasivo de CSPH y respalda su adopción en la práctica clínica.
- El SSM alcanzó una alta tasa de éxito de aproximadamente el 94%, con un rendimiento diagnóstico no afectado por la variabilidad en las mediciones (IQR).
- Los criterios de Baveno VII, que se basan en LSM y recuento de plaquetas, conducen a una proporción sustancial de pacientes en la zona “gris” de incertidumbre diagnóstica. Esto puede reducirse incorporando el SSM en algoritmos secuenciales o combinados con LSM y recuento de plaquetas.
- El algoritmo universal de estratificación del riesgo en el punto de atención desarrollado abordó las limitaciones de los criterios de Baveno VII, permitiendo su aplicación en pacientes con MASLD y obesidad.
En este estudio multicéntrico europeo de pacientes con cACLD, predominantemente debido a enfermedades metabólicas, el SSM mediante VCTE™ a 100 Hz mejoró significativamente el diagnóstico no invasivo de CSPH en comparación con los métodos estándar. El modelo integral (NICER), que incorpora SSM, LSM, recuento de plaquetas e IMC, establece un nuevo estándar para la estratificación del riesgo de CSPH, mejorando el acceso a tratamientos modificadores de la enfermedad para estos pacientes.